Lập phương trình hoá học
Một trong những phương trình thể hiện phản ứng hoá học chính xác nhất đó chính là phương trình hoá học. Vậy cách lập phương trình hoá học ra sao cũng như là những hướng giải quyết các bài tập lập phương trình hoá học như thế nào? Mời các bạn cùng với bacdau.vn đi giải quyết những thắc mắc này nhé!
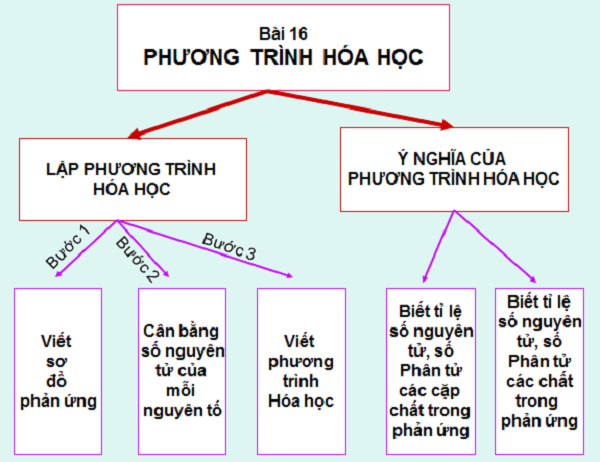
Phương trình hoá học và cách giải
Quy trình lập phương trình hoá học
Bước 1: Viết sơ đồ phản ứng, gồm công thức hóa học của các chất tham gia sản phẩm.
Bước 2: Cân bằng số nguyên tử mỗi nguyên tố: tìm hệ số thích hợp đặt trước công thức.
Bước 3: Viết thành phương trình hóa học.
Lưu ý: Bạn không nên thay đổi các chỉ số trong công thức hoá học. Viết các hệ số cao bằng kí hiệu hoá học. Đối với công thức hoá học có trong các nhóm nguyên tử như SO4 hay OH … thì coi cả hợp chất là 1 đơn vị để cân bằng, còn ở trước và sau phản ứng số nhóm nguyên tử phải bằng nhau.
Ý nghĩa của phương trình hoá học là các phương trình háo học sẽ cho chúng ta biết tỷ lệ số nguyên tử, số phân tử giữa các hợp chất cũng như là các cặp chất trong quá trình phản ứng.
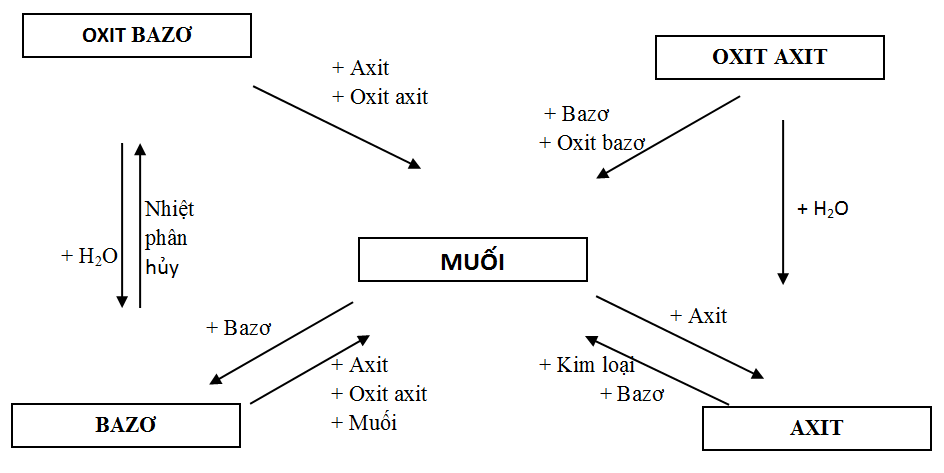
Các phương pháp cân bằng cụ thể để lập phương trình hóa học
+ Phương pháp nguyên tử nguyên tố: Phương pháp này khá đơn giản. Khi cân bằng ta cố ý viết các đơn chất khí (H2, O2, C12, N2…) dưới dạng nguyên tử riêng biệt rồi lập luận qua một số bước.
+ Phương pháp hoá trị tác dụng: Hóa trị tác dụng là hóa trị của nhóm nguyên tử hay nguyên tử của các nguyên tố trong chất tham gia và tạo thành trong PUHH.
+ Phương pháp dùng hệ số phân số: Đặt các hệ số vào các công thức của các chất tham gia phản ứng, không phân biệt số nguyên hay phân số sao cho số nguyên tử của mỗi nguyên tố ở hai vế bằng nhau. Sau đó khử mẫu số chung của tất cả các hệ số.
+ Phương pháp chẵn lẻ: Một phản ứng sau khi đã cân bằng thì số nguyên tử của một nguyên tố ở vế trái bằng số nguyên tử nguyên tố đó ở vế phải. Vì vậy nếu số nguyên tử của một nguyên tố ở một vế là số chẵn thì số nguyên tử của nguyên tố đó ở vế kia phải chẵn. Nếu ở một công thức nào đó số nguyên tử của nguyên tố đó còn lẻ thì phải nhân đôi.
+ Phương pháp xuất phát từ nguyên tố chung nhất: Chọn nguyên tố có mặt ở nhiều hợp chất nhất trong phản ứng để bắt đầu cân bằng hệ số các phân tử.
+ Phương pháp cân bằng electron: Đây là phương pháp cân bằng áp dụng cho các phản ứng oxi hóa khử. Bản chất của phương trình này dựa trênm nguyên tắc Trong một phản ứng oxi hóa – khử, số electron do chất khử nhường phải bằng số electron do chất oxi hóa thu.
Bài tập vận dụng khi lập phương trình hóa học
Bài 1: Cân bằng và lập phương trình hóa học dưới đây
1) Cu(OH)2 + HCl → CuCl2 + H2O
2) FeO + HCl → FeCl2 + H2O
3) Cu(NO3)2 + NaOH → Cu(OH)2 + NaNO3
4) N2 + O2 → NO
5) NO2 + O2 + H2O → HNO3
6) N2O5 + H2O → HNO3
7) Al2 (SO4)3 + NaOH → Al(OH)3 + Na2SO4
8) CaO + H2O → Ca(OH)2
9) Na + H3PO4 → Na2HPO4 + H2
10) Na + H3PO4 → NaH2PO4 + H2
11) C4H10 + O2 → CO2 + H2O
12) C6H5OH + Na → C6H5ONa + H2
Lời giải
1) Cu(OH)2 + 2HCl → CuCl2 + 2H2O
2) FeO + 2HCl → FeCl2 + H2O
3) Cu(NO3)2 + 2NaOH → Cu(OH)2 + 2NaNO3
4) N2 + O2 → 2NO
5) 4NO2 + O2 + 2H2O → 4HNO3
6) N2O5 + H2O → 2HNO3
7) Al2 (SO4)3 + 6NaOH → 2Al(OH)3 + 3Na2SO4
8) CaO + H2O → Ca(OH)2
9) 2Na + H3PO4 → Na2HPO4 + H2
10) 2Na + 2H3PO4 → 2NaH2PO4 + H2
11) 2C4H10 + 13O2 → 8CO2 + 10H2O
12) 2 C6H5OH + 2Na → 2C6H5ONa + H2
Hi vọng với những chia sẻ trên về lập trình phương pháp hoá học. Hi vọng bạn sẽ giúp bạn bổ sung thêm được ít kiến thức và có những thời gian vui vẻ bên BacDau.Vn nhé